Lección 8: resumen

Para detener la reproducción y crecimiento de microorganismos patógenos que pueden derivar en enfermedades, se ha de emplear métodos de destrucción o desactivación de los mismos.
En el ámbito de la limpieza y la desinfección se utilizan la esterilización y la desinfección propiamente dicha. Aunque son procesos interrelacionados, no son iguales. Veamos sus diferencias:
La esterilización consigue acabar con todos los microorganismos y con sus formas de resistencia (como las esporas), mientras que la desinfección es selectiva, solo destruye a algunas especies.
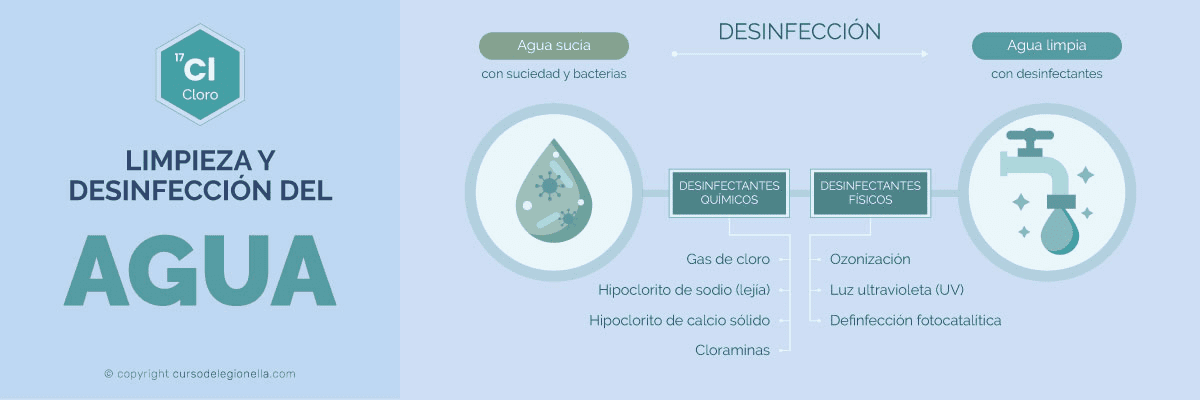
Los desinfectantes pueden ser químicos o físicos.
En la lección completa desarrollaremos las ventajas y desventajas del uso de cada uno de los desinfectantes.
Los principales desinfectantes químicos son:
- Gas de cloro.
- Cloración (hipoclorito de sodio).
- Cloración (hipoclorito de calcio sólido).
- Cloraminas.
Los principales desinfectantes físicos son:
- Ozonización.
- Luz ultravioleta (UV).
- Desinfección fotocatalítica.
Lección 8: ampliada
Métodos generales de limpieza y desinfección
Principales desinfectantes químicos
En la actualidad existen en el mercado una gran variedad de sustancias desinfectantes que son empleadas para reducir la presencia de Legionella pneumophila en las instalaciones. Algunas de las más empleadas son las siguientes:
Gas de cloro:
El cloro es un gas de color amarillo verdoso. Al proporcionar alta presión, el gas se vuelve líquido. Es tóxico. El cloro gaseoso se utiliza principalmente como desinfectante de agua. La introducción de cloro en el agua juega un papel muy poderoso para eliminar casi todos los microorganismos patógenos.
El gas no es aplicable para ser utilizado en el sistema doméstico ya que es muy peligroso. Es letal en concentraciones tan bajas como 0,1% de aire por volumen.
Ventajas:
- La cloración es una fuente más barata que los métodos de desinfección con ozono o UV utilizados para tratar el agua.
- Es muy eficaz contra una amplia gama de microorganismos patógenos.
- Los residuos de cloro que quedan en el efluente de las aguas residuales pueden prolongar el proceso de desinfección incluso después del tratamiento inicial.
Inconvenientes:
- Desarrolla malos sabores y olores al agua.
- Limitaciones en el uso de cloro gaseoso en un contexto doméstico al ser tóxico.
- Peligros para la salud causados por los productos resultantes de la cloración del agua. Se ha identificado en muchos estudios que algunos de estos cloro-orgánicos son mutágenos, toxinas o carcinógenos.
Cloración (hipoclorito de sodio):
El hipoclorito de sodio (más conocido como lejía) se utiliza como agente blanqueador, principalmente para blanquear textiles, y como desinfectante líquido.
La solución generalmente contiene entre el 10% y el 15% del cloro disponible, pero pierde rápidamente su fuerza en el proceso de almacenamiento.
Se necesita un ambiente controlado y regular ya que la solución se ve muy afectada por el pH, la luz, el calor y los metales pesados.
Ventajas:
- El hipoclorito de sodio también se puede utilizar como desinfectante.
- Tanto el hipoclorito de sodio como el cloro gaseoso muestran una eficacia de desinfección similar.
- En comparación con el cloro gaseoso, la desinfección con hipoclorito de sodio reduce los peligros de almacenamiento y manipulación.
- No se utilizan productos químicos peligrosos en la generación in situ. Solo se usa agua y sal de alto grado (NaCl).
- En comparación con la solución estándar suministrada (concentración del 14%), las soluciones de hipocloruro de sodio son menos peligrosas (concentración del 1%) y están menos concentradas mientras generan producción in situ.
Inconvenientes:
- El hipoclorito sódico puede suministrarse comercialmente o generarse in situ, siendo este último el más seguro de los dos métodos por motivos de manipulación.
- En la generación in situ, la sal se disuelve con agua blanda para formar una solución de salmuera concentrada que posteriormente se diluye y pasa a través de una celda electrolítica para formar hipoclorito de sodio.
- El hidrógeno también se produce durante la electrólisis y es necesario ventilarlo debido a su naturaleza explosiva.
Cloración (hipoclorito de calcio sólido):
El hipoclorito de calcio es un producto sólido que puede usarse en reemplazo del hipoclorito sódico (líquido).
Como desinfectante, tiene similitud con el hipoclorito sódico, pero es mucho más seguro de manejar.
Tiene un 70% de cloro y tiene aplicaciones tanto en aguas residuales como en agua potable.
Ventajas:
- Al ser sólido es más seguro que el cloro gaseoso y el hipoclorito sódico.
- Incluso tiene una excelente estabilidad cuando se almacena en lugar seco, manteniendo bien su potencia en el tiempo.
Inconvenientes:
- La contaminación o su uso inadecuado puede provocar una explosión, un incendio o la liberación de gases tóxicos. No se debe permitir que el hipoclorito de calcio entre en contacto con materias extrañas (incluidos otros productos para el tratamiento del agua).
- Si está expuesto incluso a cantidades muy pequeñas de agua, puede reaccionar violentamente para producir gases tóxicos, calor y salpicaduras. El producto debe agregarse al agua en lugar de agregar agua al producto.
- La exposición al calor puede hacer que se descomponga rápidamente, lo que puede provocar una explosión, un incendio intenso y la liberación de gases tóxicos. Se necesita un área seca, fresca y bien ventilada para almacenar el producto.
- Aumenta la intensidad del fuego. Debe mantenerse alejado del calor, es decir, las llamas, el calor y cualquier tipo de material en combustión.
Cloraminas:
Las cloraminas se forman al hacer reaccionar el amoníaco con cloro libre. Desempeñan un papel importante a la hora de proporcionar protección residual en el sistema de distribución de agua. Son muy estables.
En comparación con el cloro, se forman menos subproductos halogenados.
Ventajas:
- No se forman subproductos en la cloraminación.
Inconvenientes:
- La cloramina es más estable pero no es un desinfectante fuerte como el cloro, proporcionando un desinfectante residual de larga duración.
Principales Desinfectantes Físicos
Ozonización:
El ozono es una fórmula inestable de oxígeno en la que se combinan tres moléculas para producir una nueva. Se descompone rápidamente para generar radicales libres altamente reactivos. El potencial de oxidación del ozono es mayor que el del cloro o el ion hipoclorito, sustancias muy utilizadas en el tratamiento de aguas residuales como los oxidantes. El ozono es superado solo por el radical hidroxilo y el fluoruro en su capacidad de oxidación.
Ventajas:
- El ozono posee un fuerte poder oxidante.
- Se necesita un tiempo de reacción corto para que los gérmenes (incluidos los virus) se eliminen en unos pocos segundos.
- No se producen cambios de color y sabor.
- No requiere productos químicos.
- Se proporciona oxígeno al agua después de la desinfección.
- Destruye y elimina las algas.
- Oxida el hierro y el manganeso.
- Reacciona y elimina toda la materia orgánica.
Inconvenientes:
- La generación in situ es necesaria ya que el ozono es inestable a la presión atmosférica.
- Es tóxico en altas concentraciones ya que es un gas de efecto invernadero.
Luz ultravioleta (UV):
El tratamiento UV se puede utilizar para tratar aguas residuales, agua potable y acuicultura. La luz ultravioleta provoca la desinfección al cambiar los componentes biológicos de los microorganismos rompiendo específicamente los enlaces químicos en el ADN, el ARN y las proteínas.
Ventajas:
- Limita el rebrote potencial dentro del sistema de distribución por lo que no se produce un aumento en la concentración de carbono orgánico biodegradable o asimilable.
- No se forman subproductos.
- Mediante el uso de luz ultravioleta podemos lograr la misma inactivación de parásitos como Giardia y Cryptosporidium, con un costo menor que las técnicas de dióxido de cloro y ozono.
- Cuando se usa en relación con cloraminas, no se nota la formación de subproductos de desinfección clorados.
Inconvenientes:
- En los países subdesarrollados, existen varias limitaciones para la desinfección UV. La mayor limitación es el requerimiento de energía.
- Solo es eficaz como desinfectante primario ya que no deja residuos. No actúa como desinfectante secundario ya que no actúa contra la reinfección en el agua.
- Una preocupación con respecto a la desinfección UV es la composición química y la calidad de los microorganismos presentes en el agua afluente.
Desinfección fotocatalítica:
La aceleración de una fotorreacción en presencia de un catalizador se denomina fotocatalizador. En la fotólisis catalizada, se utiliza un sustrato para absorber la luz.
Su aplicación práctica fue posible gracias al descubrimiento de la electrólisis del agua mediante el uso de dióxido de titanio.
Ventajas:
- La fotocatálisis utiliza la capacidad de energía solar renovable y libre de contaminación, por lo que es un buen sustituto de los métodos de tratamiento convencionales que consumen mucha energía.
- En comparación con los métodos de tratamiento convencionales, la fotocatálisis conduce a la formación de compuestos inocuos.
- Las aguas residuales contienen diferentes compuestos peligrosos. El proceso fotocatalítico provoca la destrucción de una amplia gama de estos compuestos peligrosos en varias corrientes de aguas residuales.
- Estas reacciones son leves. Se requiere menos aporte químico y el tiempo de reacción es reducido.
Inconvenientes:
- TiO2 tiene poca afinidad por los contaminantes orgánicos, por lo que la adsorción de contaminantes orgánicos en la superficie del TiO2 es baja, lo que da como resultado tasas lentas de degradación fotocatalítica.
- Las nanopartículas de TiO2 pueden sufrir agregación, lo que puede provocar la reducción de la actividad catalítica. Sin embargo, debe tenerse en cuenta que puede suceder que pequeñas partículas muestren mayor dispersión, lo que puede reducir su actividad fotocatalítica en comparación con las más grandes.
- Es un modo de desinfección muy caro



